Número de saponificación
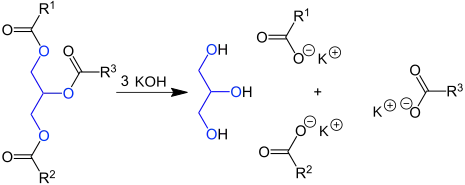
El índice de saponificación o número de saponificación (SV o SN, de las siglas en inglés) es la cantidad de miligramos de hidróxido de potasio (KOH) o hidróxido de sodio (NaOH) necesarios para saponificar un gramo de grasa en las condiciones especificadas.[1][2] Es una medida del peso molecular promedio (o longitud de cadena) de todos los ácidos grasos presentes en la muestra como triglicéridos. Cuanto mayor sea el índice de saponificación, menor será la longitud media de los ácidos grasos, menor será el peso molecular medio de los triglicéridos y viceversa. En la práctica, las grasas o los aceites con alto valor de saponificación (como el aceite de coco y de palma) son más adecuados para la fabricación de jabón.
Determinación
Para determinar el valor de saponificación, la muestra se saponifica en caliente con un exceso de álcali (generalmente hidróxido de potasio disuelto en etanol ), en condiciones estándar, generalmente durante media hora a reflujo . El álcali es consumido principalmente por los glicéridos: triglicéridos, diglicéridos, monoglicéridos, pero también por los ácidos grasos libres, así como por otros componentes similares a los ésteres, como las lactonas.[3] Al final de la reacción, la cantidad restante de álcali se valora frente a una solución estándar de ácido clorhídrico (HCl). Por lo tanto, el SV (mg KOH/g de muestra) se calcula de la siguiente manera:
|
(1) |
Donde : (B - S) es la diferencia entre el volumen de solución de HCl utilizado para la corrida en blanco y para la muestra analizada, en mL;
M es la molaridad de la solución de HCl, en mol · L−1;
56,1 es el peso molecular de KOH, en g · mol-1;
W es el peso en peso de la muestra, en g.
El SV también se puede calcular a partir de la composición de ácidos grasos determinada por cromatografía de gases.
Índices de saponificación de varios aceites y grasas
| Grasa | Índice de saponificación (mg KOH/g)[4][5] | Materia insaponificable (%)[4][6] |
|---|---|---|
| Cera de abeja | 60 – 102 | > 52 |
| Aceite de colza (Brassica napus) | 182 – 193 | < 0,2 |
| Manteca de cacao | 192 – 200 | 0,2 – 1 |
| Aceite de coco | 248 – 265 | 0,1 – 1.4 |
| Aceite de maíz | 187 – 195 | 1 – 3 |
| Aceite de algodón | 189 – 207 | < 2 |
| Aceite de pescado[7] | 179 – 200 | 0,6 – 3 |
| Lanolina[8][9] | 80 – 127 | 40 – 50 |
| Manteca de cerdo[10] | 192 – 203 | < 10 |
| Linaza | 188 – 196 | 0,1 – 2 |
| Aceite mineral | 0 | 100 |
| Aceite de oliva | 184 – 196 | 0,4 – 1.1 |
| Aceite de semilla de palma | 230 – 254 | < 1 |
| Aceite de palma | 190 – 209 | < 1,4 |
| Aceite de cacahuete | 187 – 196 | 0,2 – 4.4 |
| Aceite de colza (Brassica rapa) | 168 – 181 | 0,7 – 1.1 |
| Aceite de cártamo | 188 – 194 | < 1,6 |
| Manteca de karité | 170 – 190 | 6 – 17 |
| Aceite de soja | 187 – 195 | 1,5 – 2.5 |
| Aceite de girasol | 189 – 195 | 0,3 – 1.2 |
| Aceite de ballena[3] | 185 – 202 | < 2 |
| Aceite de ricino | 170 – 210 |
Los insaponificables son componentes de una sustancia grasa (aceite, grasa o cera) que no forman jabones cuando se tratan con álcali y permanecen insolubles en agua pero solubles en disolventes orgánicos. Por ejemplo, el aceite de soja típico contiene, en peso, entre un 1,5 y un 2,5 % de materia insaponificable. Los insaponificables incluyen componentes no volátiles: alcanos, esteroles, triterpenos, alcoholes grasos, tocoferoles y carotenoides, así como los que resultan principalmente de la saponificación de ésteres grasos (ésteres de esteroles, ésteres de cera, ésteres de tocoferoles...). Esta fracción también puede contener contaminantes ambientales y residuos de plastificantes, pesticidas, hidrocarburos de aceites minerales y aromáticos.[11]
Referencias
- ↑ «Saponification Value of Fats and Oils». Consultado el 18 de enero de 2018.
- ↑ Klaus Schumann, Kurt Siekmann (2005). «Soaps». Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. ISBN 3527306730. doi:10.1002/14356007.a24_247.
- 1 2 Chakrabarty, M. M. (2003). Chemistry and Technology of Oils & Fats (en inglés). New Delhi: Allied Publishers. pp. 89, 183. ISBN 978-81-7764-495-1.
- 1 2 Gunstone, Frank (2009). Oils and Fats in the Food Industry (en inglés). John Wiley & Sons. ISBN 978-1-4443-0243-1.
- ↑ Akoh, Casimir C.; Min, David B. (2008). Food Lipids: Chemistry, Nutrition, and Biotechnology, Third Edition (en inglés). CRC Press. ISBN 978-1-4200-4664-9.
- ↑ «Physical Properties of fats and Oils». Deutsche Gesellschaft für Fettwissenschaft e.V. Consultado el 14 de septiembre de 2020.
- ↑ Turchini, Giovanni M.; Ng, Wing-Keong; Tocher, Douglas Redford (2010). Fish Oil Replacement and Alternative Lipid Sources in Aquaculture Feeds (en inglés). CRC Press. ISBN 978-1-4398-0863-4.
- ↑ «Lanolin - CAMEO». cameo.mfa.org. Consultado el 14 de septiembre de 2020.
- ↑ Wilkie, John M. (1917). «The estimation of unsaponifiable matter in oils, fats, and waxes». Analyst (en inglés) 42 (495): 200-202. Bibcode:1917Ana....42..200W. ISSN 1364-5528. doi:10.1039/AN9174200200.
- ↑ «SECTION 3. Codex Standard for Fats and Oils from Animal Sources». www.fao.org. Consultado el 14 de septiembre de 2020.
- ↑ Belitz, H.-D.; Grosch, Werner; Schieberle, Peter (2013). Food Chemistry (en inglés). Springer Science & Business Media. ISBN 978-3-662-07279-0.